
医药行业

一、云顶集团7610医药行业产品的应用场景
(US FDA) 21 CFR Part 11 美国联邦法规21篇第11部分 电子记录与电子签名
(US FDA) 工业指南11部分 电子记录与电子签名-范围和应用
(ISPE) 良好自动化生产实践指南,遵从GXP计算机化系统监管的风险管理方案
(ISPE) GAMP GPG良好实践指南,GAMP架构下的系列良好实践指南
(EU) 欧盟药事法规第4卷GMP,附录11《计算机化系统》
(TGA)GMP,药用产品良好生产实践指南
(PIC/S)在“GxP”监管环境下的计算机化系统良好实践(检察官指南)
WHO TRS1019 53号报告-Annex3-Guidelines on Validation
WHO TRS1019 53号报告-Annex3-Appendix 5 Validation of computerized systems
(CFDA) 2010年版GMP及附录《计算机化系统》
(CFDA) GSP附录二附录三《药品经营企业计算机系统》《温湿度自动监测》
医药产业链模型,随着“两票制”全国推行,医药经营多级批发商的时代将发生重大变革
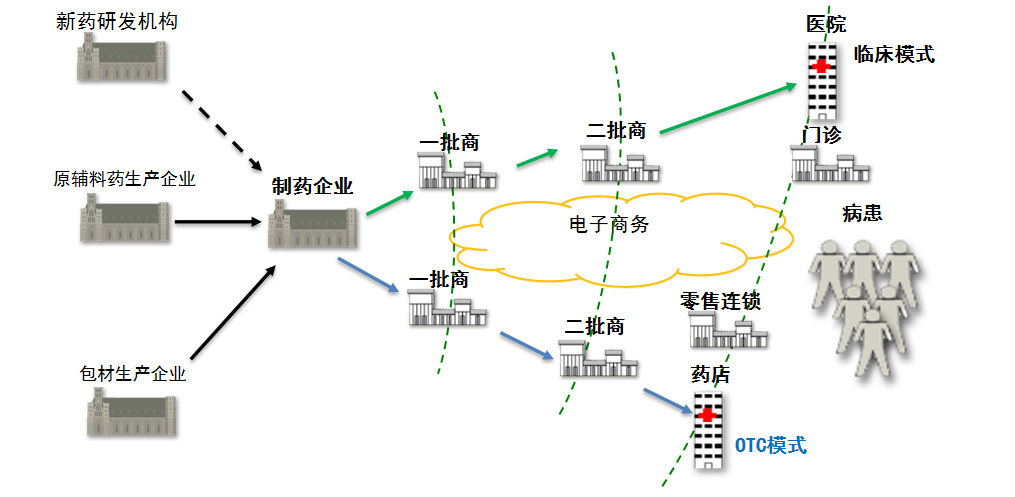
二、医药产业网链企业管理场景说明
药品批号:生产单位在药品生产过程中,将同一次投料、同一次生产工艺所生产的药品用一个批号来表示。
处方药:是必须凭执业医师或执业助理医师处方才可调配、购买和使用的药品。
OTC药:是不需要凭医师处方即可自行判断、购买和使用的药品。
终端: 第一终端:大型医院;第二终端:药店;第三终端:乡镇医院及诊所。
医院纯销:是指医院实际销售出去的销量,即上月库存量+本月进货-本月库存=纯销。
统方:医生的处方被药房收下后,是要被统计、保留几年的,你的品种根据药房人员对处方的统计得到每个月、每个医生实际开出多少。
两票制:是指药品生产企业产品通过一级经销商直接配送给医院并开具发票,一级经销商必须直接从生产商购货、结算,由生产商直接对经销商开具发票。国家新的医改方案对基本药物实现定点生产、专门配送实际上就是实现“两票制”。
三、新版GSP针对计算机系统关键要求
(1)新版GSP要求一
内嵌式结构:
是指医药经营企业的采购、销售、收货、验收、储存、运输这些环节的管理,软件要是一体化的,不能分拆,前后环节之间,数据是自动流转的,有严格的钩稽关系的。例如:
♦ 采购收货:【采购订单】是采购收货的“供应商、品种、数量”控制依据,没有采购订单,软件不允许进行收货操作。
♦ 销售退回验收:【销售退回申请】生成的【销售退回验收通知单】是销退收货的“客户、品种、数量、批号”的控制依据,销售退回验收通知单中没有列出的品种及批号数量,软件不允许进行销售退回验收操作。
♦ 采购发票:严格钩稽采购入库单,没有入库单,不能形成采购发票。
♦ 业务ERP数据能够与“财务软件”无缝对接,数据有严格钩稽关系。
非内嵌式结构:
♦ 模块之间独立
♦ 系统外挂
♦ 数据分离
♦ 没有数据间的钩稽控制关系。
(2)新版GSP要求二
识别及控制:是指医药经营企业的采购、销售、收货、验收、储存、养护、出库复核、运输这些环节的管理,软件要能够根据设置的管控条件,自动判断是否超出范围经营、证照过期是否可以自动控制、商品过期是否自动控制等。例如:
♦ 采购订单:超出供应商经营范围的品种,不允许购进;超出供应商业务员授权委托书期限的,不允许购进;供应商证照(大证。营业执照及年检期限、组织机构代码证年检期限)过期的,不允许购进;供应商专项证照(专项证。例如:药品经营许可证、医疗器械经营许可证、食品流通许可证等)过期的,对应的品种不允许购进;生产企业的,对应品种的GMP证书、批准文号期限、进口注册证期限等过期的,不允许购进;
♦ 销售开单:超出客户经营范围的品种,不允许销售;客户证照(大证。营业执照及年检期限、组织机构代码证年检期限)过期的,不允许销售;客户专项证照(专项证。例如:医疗执业许可证、药品经营许可证、医疗器械经营许可证、食品流通许可证等)过期的,对应的品种不允许销售;
控制功能的实时及有效:
是指软件要能够根据设置的管控条件,在快到期限的时候,能够预警相关人员,在达到控制条件时,系统能直接“阻挡”。例如:
♦ 采购验收:没有采购订单的不能验收,验收合格数量不能超过订单数量;在出现需要扫描电子监管码商品时,系统能够及时提醒,没有扫描不能下行;如果是进口药品,没有批次检验报告单,不能下行;如果是需要双人验收商品,第二验收人员没有操作不能下行;不符合企业效期规定的记录进入验收待查内,等待采购部门确认等等;
♦ 销售退回:【销售退回申请】只能从历史销售记录内引入形成,并且不能超过原销售数量;销售退回验收通知只能由【销售退回申请单】生成,并且验收时自能按通知的批号收货验收、数量不能超过通知的数量等等。
(3)新版GSP要求三
拦截:
是指当控制条件满足时,软件要能够自动阻挡流程的下行。例如:
进口药品没有批次检验报告,不能验收下行;
过期失效商品、不合格品在销售开单时可以拦截。
预警:
主要是指软件自动提醒,例如“药品近效期提醒、证照快到失效期等、温湿度达到预警设置提醒等”。预警的方式一般采用滚动提醒方式。
提醒:
主要是指消息的提醒、工作内容的提醒等。一般也是采用滚动提醒方式。
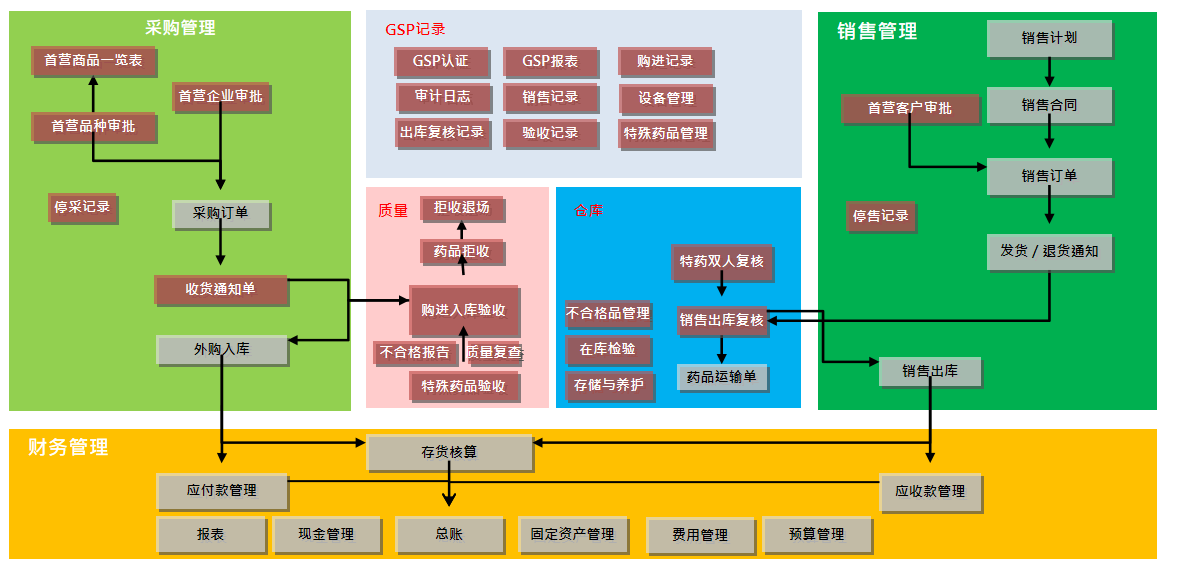
四、云顶集团7610医药流通GSP总体业务流程
云顶集团7610医药流通GSP功能介绍:
♦ 关键应用一:首营管理及预警控制
♦ 关键应用二:供应链出入质量管控
♦ 关键应用三:存储与养护
♦ 关键应用四:质量反馈及控制机制
♦ 关键应用五:设备管理及员工管理
♦ 关键应用六:数据分析及审计控制
五、云顶集团7610医药首营管理业务需求与应用场景
为了确保企业经营行为的合法性,保证药品购进质量,医药流通企业在购进药品时,与本企业首次发生供需关系的药品生产或经营企业,需要进行首营企业审批,并对于从生产厂家采购的药品,需要进行首营品种审批,对与本企业首次发生供需关系的销售客户,也需要进行首营客户审批,在首营审批时,必须提供加盖企业原印章的合法证照复印件;药品销售人员需提供身份证复印件,及加盖企业原印章和企业法定代表人印章或签字的授权委托书,并标明委托授权范围及有效期,还应提供首营企业质量认证情况的有关证明。
通过对首营企业、首营品种、首营客户的审批管理,确保企业经营符合法规要求,在进行首营企业登记时,可对营业执照、生产/经营许可证、授权委托书、质量保证协议、生产/经营范围同时进行监管,并根据各企业特色可设置管控的严格度;首营客户登记时,对客户的营业执照及药品经营许可证进行监管;首营品种登记时,对首营品种的产品注册证和药品GMP证书进行监管。用户可根据业务需要增加自定义的证照经行监管。在采购业务、销售业务的流程中对未通过首营审批、证照过期、无经营权等进行检查控制,有效防止非法经营,杜绝安全隐患。可以真正严格有效地将GSP 管理的质量要求切实履行于业务活动中,对于及时发现质量问题,避免质量事故,降低企业经营风险起着不可估量的巨大作用。
六、新版GMP特点
♦ 吸收国际先进经验。
♦ 重点细化软件要求
加强了药品生产质量管理体系建设,大幅提高对企业质量管理软件方面的要求
♦ 全面强化从业人员的素质要求
♦ 细化文件管理规定
随着计算机程控化系统的广泛使用,新版GMP增加了电子记录管理的内容。
♦ 进一步完善药品安全保障措施
♦ 引入或明确了一些概念
如:质量授权人、质量风险管理、变更管理、偏差管理、纠正和预防措施、超标结果调查等。
七、质量管理体系建设中的重点和难点问题
在贯彻实施新版GMP的过程中,大家遇到的难点,除了生产硬件条件的提高外,重点就是质量管理体系的建设。
怎样准确理解、把我质量管理体系构成要素?
♦ 偏差、变更、投诉、纠正和预防(CAPA)、OOS等管理流程,是否合规、有效,如何进一步改进?
♦ 怎样确保质量控制与质量保证的有效性,如何进一步提升企业的质量管理水平?
♦ 怎样进行有效的质量追踪,是否建立了偏差,变更,OOS等重要管理流程之间的关联和制约关系?
♦ 怎么样建立有效的风险管理流程?如何将风险管理与偏差、变更等其他质量管理要素进行有效的结合,从而保证其科学性、合理性,并能够根据风险等级进行风险的处理?
八、客户体验反馈-云南白药
云南白药前身为成立于1971年 6月的云南白药厂。1996年公司更名为云南白药集团股份有限公司。
经过30多年的发展,云南白药已从一个资产不足300万元的生产企业成长为一个总资产100亿多,总销售收入逾243亿元(2017年末),经营涉及化学原料药、化学药制剂、中成药、中药材、生物制品、保健食品、化妆品及饮料的研制、生产及销售;医疗器械(二类、医用敷料类、一次性使用医疗卫生用品),日化用品等领域的云南省实力最强、品牌最优的大型医药企业集团。
需求背景:云南白药从“新白药大健康”战略的高度对事业部信息化做出新的规划,搭建统一全渠道营销的信息化平台,实现终端客户及经销商管理、实现事业部统一管控标准、实现业务财务的一体化、加强对内部事业部的精细化考核;移动互联网时代的来临对信息系统提出的新的挑战,其中GSP与供应链的整合是其信息化搭建的至关重要的一步。


